随着研究者将免疫检查点作为抗击癌症的新靶点后的不断探索,IDO抑制剂逐渐浮出了水面,成为该领域的另一个新的分支。现在有关IDO抑制剂的临床试验表明,其联合PD-1/PD-L1抑制剂治疗有着良好的前景。
作用机制
IDO蛋白是一种免疫检查点蛋白,与在肿瘤微环境中产生免疫抑制作用,支持肿瘤生长。该酶有两种亚型,分别为IDO1和IDO2,在该代谢通路中的第一步——分解色氨酸中起到重要作用。
IDO通过抑制T细胞的效应器功能发挥其免疫调节作用。上调IDO蛋白的水平可以导致生长停滞和效应T细胞(细胞毒T细胞、辅助T细胞、NK细胞等)的凋亡。而效应T细胞数量下降自然就保护了癌细胞受到攻击。
研发人员发现,IDO在肿瘤细胞及其附近的微环境的细胞中均有表达,如在肿瘤浸润淋巴结中的DC细胞(如下图)。这提供给药物研发人员针对IDO信号通路研发药物的机会。
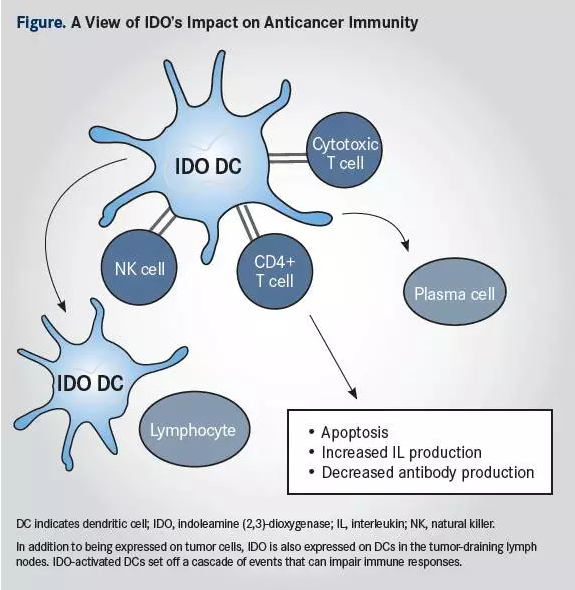
在很多实体瘤种,IDO均有表达的情况。这驱使着药物研发人员开展了很多IDO抑制剂的临床试验。现在,至少5个IDO抑制剂正在联合免疫治疗药物或化疗开展临床研究(如下表)。
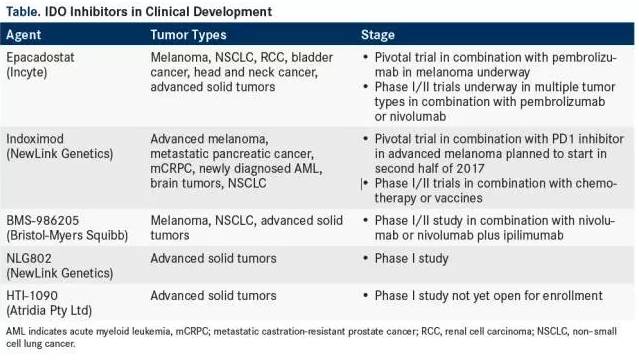
现在这些IDO抑制剂正在开展的临床试验的结果表明,其联合PD-1抑制剂的毒性较低。这对于免疫联合治疗这条出路无疑是个好消息,现在已经陆续开展Ⅱ期临床研究了。
Epacadostat
开展研究最快的IDO抑制剂为Epacadostat,一种口服的IDO抑制剂。Epacadostat的早期试验结果比较令人满意,尤其在黑色素瘤中,该药正在分别联合pembrolizumab和nivolumab进行临床试验。
在其联合pembrolizumab的Ⅰ期研究中纳入了初治的黑色素瘤患者,58%(11/19)的患者接受IDO抑制剂及PD-1抑制剂达到了客观缓解。其中26%的患者达到CR,32%患者达PR。
疾病控制率(DCR,包括CR, PR, SD患者)达到了74%。
该联合方案的成功促成了Ⅲ期研究的开展。现在正在进行的KEYNOTE-252/ECHO-301研究将随机纳入600例既往未接受过治疗的转移性或不可切除黑色素瘤患者,接受pembrolizumab联合或不联合epacadostat治疗。
同样的,在ASCO 2017上报道的ECHO-204的Ⅰ/Ⅱ期研究中,epacadostat联合nivolumab也在黑色素瘤患者中得到了良好的结果,其ORR率为63%,CR率为5%。
Epacadostat联合PD-1抑制剂在其他实体瘤中也起到了较好的疗效。在正在进行的Ⅰ/Ⅱ期ECHO-202/KEYNOTE 037研究中表明,在转移性或复发性头颈鳞癌患者中,epacadostat联合PD-1抑制剂可以达到34%的ORR(13/38),进展期尿道细胞癌中为35%(14/40),转移性肾细胞癌为33%(10/30)。
安全性方面,一个294例患者的合并分析表明,治疗相关副反应发生率为67%,3度以上副反应发生率仅为18%。最常见的副反应为疲乏(29%)、红疹(17%)、恶心(11%)和瘙痒(10%)。4%的患者由于治疗相关副反应停药。
Nivolumab方面,ECHO-204研究表明Nivolumab联合epacadostat在头颈鳞癌治疗中的ORR为23%,CR率为3%。
Indoximod
Indoximod是一个直接逆转IDO抑制免疫细胞的小分子化合物,在早期的临床试验中也观测到了较强的活性。AACR 2017上的汇报的结果表明,其联合PD-1抑制剂可获得52%的ORR。
NLG 2103研究是一个单臂的临床研究,探究Indoximod根据医生选择联合ipilimumab,nivolumab,pembrolizumab其中一个治疗不可切除的Ⅲ/Ⅳ期黑色素瘤。
截止到2017年3月,共入组102名患者。其中94例接受pembrolizumab治疗,8例接受nivolumab或ipilimumab治疗。在AACR大会上,共报道了60例可评估患者的数据。
整组的客观缓解率为52%(31/60),其中CR6例(10%),PR25例(42%)。SD患者占22%,PD患者占27%。
将眼部黑色素瘤剔除后,ORR,CR和PR率分别为59%,12%和47%。最常见的全级不良反应为乏力(60%),头痛(33%),恶心(32%),关节痛(28%),腹泻(28%),瘙痒(26%),红疹(23%)和咳嗽(21%)。3度以上不良反应分别为乏力、腹泻和红疹各1例。
现在相关企业拟在2017下半年进行IDO抑制剂联合PD-1抑制剂的Ⅲ期临床研究。
该药物也在联合希普鲁塞在转移性去势抵抗前列腺癌中进行临床研究。结果表明实验组的PFS为10.3个月,对照组为4.1个月(p=0.011)。
新兴的IDO抑制剂
其他正在进行研发的IDO抑制剂中,BMS-986205传递出了较好的信号。前临床研究的结果表明,BMS-986205可以抑制IDO1,恢复T细胞的分化,降低免疫抑制代谢性犬鸟氨酸水平。
在Ⅰ/Ⅱ期临床试验中,BMS-986205在既往治疗过的肿瘤中进行剂量爬坡试验,已从25mg每天提升至200mg每天。
该研究中单药BMS-986205提前应用2周后,联合nivolumab 240mg/kg,14d/cycle进行治疗。BMS-986205正在扩充宫颈癌、头颈鳞癌、膀胱癌患者的队列。在13名患者中均观测到了肿瘤内犬尿氨酸水平的降低。
现在,该研究已经发展成联合nivolumab或nivolumab+ipilimumab的临床试验,该Ⅰ/Ⅱ期研究拟纳入900名患者入组(NCT02658890)。
参考文献
1.Gangadhar TC, Hamid O, Smith DC, et al. Epacadostat plus pembrolizumab in patients with advanced melanoma and select solid tumors: updated phase 1 results from ECHO-202/KEYNOTE-037. Presented at: 2016 European Society for Medical Oncology Congress; October 7-11, 2016; Copenhagen, Denmark. Abstract 1110PD. www.incyte.com/ir/events-and-presentations.aspx.
2.Perez RP, Riese JM, Lewis KD, et al. Epacadostat plus nivolumab in patients with advanced solid tumors: preliminary phase I/II results of ECHO-204 [ASCO abstract 3003]. J Clin Oncol. 2017;35 (suppl). meetinglibrary.asco.org/record/153930/abstract.
3.Updated data from ECHO-202 trial of Incyte’s epacadostat in combination with Merck’s Keytruda (pembrolizumab) demonstrate clinical activity across multiple tumor types [news release]. Wilmington, DE, and Kenilworth, NJ: Incyte Corporation and Merck; June 5, 2017. incyte.com/ir/press-releases.aspx. Accessed August 8, 2107.
4.Zakharia Y, McWilliams R, Shaheen M, et al. Interim analysis of the phase 2 clinical trial of the IDO pathway inhibitor indoximod in combination with pembrolizumab for patients with advanced melanoma. [AACR abstract CT117]. Cancer Res. 2017;77(13 suppl). doi: 10.1158/1538-7445.AM2017-CT117.
5.NewLink Genetics. IDO pathway inhibitor clinical development. newlinkgenetics.com/pipeline/. Accessed August 8, 2017.
6.Gopalji Jha G, Gupta S, Tagawa ST, et al. A phase II randomized, double-blind study of sipuleucel-T followed by IDO pathway inhibitor, indoximod, or placebo in the treatment of patients with metastatic castration resistant prostate cancer (mCRPC) [ASCO abstract 3066]. J Clin Oncol. 2017;35(suppl). meetinglibrary.asco.org/ record/145096/abstract.
7.Siu LL, Gelmon K, Chu Q, et al. BMS-986205, an optimized indoleamine 2,3-dioxygenase 1 (IDO1) inhibitor, is well tolerated with potent pharmacodynamic (PD) activity, alone and in combination with nivolumab (nivo) in advanced cancers in a phase 1/2a trial. [AACR abstract CT116]. 2017;77(13 suppl). doi: 10.1158/1538-7445.AM2017-CT116.